
30g Ballaststoffe pro Tag sind laut der Deutschen Gesellschaft für Ernährung ideal. Was halten Sie von dieser Empfehlung, Herr Schwiertz?
Verglichen mit den Anfängen der Menschheit und den Naturvölkern sind 30g eine eher geringe Menge. Der Mensch ist in früherer Zeit durchschnittlich 30.000 Schritte am Tag gegangen und die Ernährung bestand zu einem Großteil aus gesammelten Pflanzen, wodurch eine Ballaststoffmenge von etwa 100g pro Tag dem Durchschnitt entsprach (https://pubmed.ncbi.nlm.nih.gov/16441938/).
Wir haben über die evolutionäre Entwicklung Bakterien als Symbionten gewonnen, die in der Lage sind, die für uns Menschen eigentlich nicht nutzbaren Ballaststoffe aufzuspalten. Wenn sie diese fermentieren, entsteht Energie in Form von kurzkettigen Fettsäuren. So können in Hungerphasen 200 bis 300 kcal zusätzlich zur Verfügung stehen, ohne dass dafür Nahrung aufgenommen werden muss. Allerdings ist dieses System in der heutigen Zeit und in unseren Teilen der Welt eher kontraproduktiv, da Mangelernährung in der Regel kein Problem darstellt. Die zusätzlichen Kalorien durch erhöhte Ballaststoffaufnahme werden also nicht mehr benötigt.
Dennoch sind Ballaststoffe ein wichtiger Baustein einer gesunden Ernährung. 30g pro Tag aufzunehmen wäre in heutiger Zeit wünschenswert. Erfahrungsgemäß kommen die meisten Menschen allerdings nicht auf diese Menge, da Zeit oder das Wissen um gesunde Ernährung fehlt.
Ist es Ihrer Meinung nach also sinnvoll, Ballaststoffe zu supplementieren?
Ich halte es nicht nur für sinnvoll, für viele Menschen ist es der einzige Weg, eine ausreichende Ballaststoffaufnahme zu gewährleisten. Andere Nährstoffmängel werden ebenso über Supplemente ausgeglichen. Wenn durch Nahrungsergänzungsmittel 30g Ballaststoffe aufgenommen werden, sehe ich das als geeigneten Weg an.
Sind diese 30g Ballaststoffe pro Tag für Sie auch der ausschlaggebende Wert für eine ‚gesunde‘ Mikrobiota?
An dieser Stelle möchte ich zunächst auf den Begriff der gesunden Mikrobiota eingehen, denn wenn Sie nicht krank sind, ist Ihre Mikrobiota per se erst einmal als gesund einzustufen, auch wenn sie - mikrobiologisch betrachtet - nicht ideal sein mag. Gefahrenpotenziale sehe ich hingegen im Zusammenhang mit der mikrobiotischen Signatur, da hier Korrelationen mit bestimmten Erkrankungen existieren. Viele Bakterien produzieren beispielsweise Neurotransmitter oder Vitamine, wie B12. Verschiedene Arten von Bakterien können dieselben Stoffe produzieren. Sollte also eine Art nicht ausreichend vorhanden sein, kann deren Funktion von einem anderen Bakterienstamm übernommen werden. Der Fokus sollte hier also auf der Funktion der Bakterien liegen und nicht unbedingt auf den spezifischen Bakterienarten.
Die Devise lautet also: Je diverser das Mikrobiom, desto besser?
Ganz genau, je diverser das Mikrobiom, desto funktionaler ist der Darm.
Kann diese Diversität durch die Ernährung direkt beeinflusst werden?
Definitiv. Auch das wird wieder deutlich am Unterschied zwischen heutigen Mitteleuropäern und Naturvölkern. Die klassischen Mitteleuropäer ernähren sich mit der so genannten Western diet omnivor, aber eher einseitig. Dadurch ist ihre Bakteriengemeinschaft ähnlich und weniger vielfältig. Naturvölker, die sich jeden Tag unterschiedlich ernähren, da sie von ihren äußeren Umständen abhängig sind, haben eine deutlich diversere Mikrobiota.
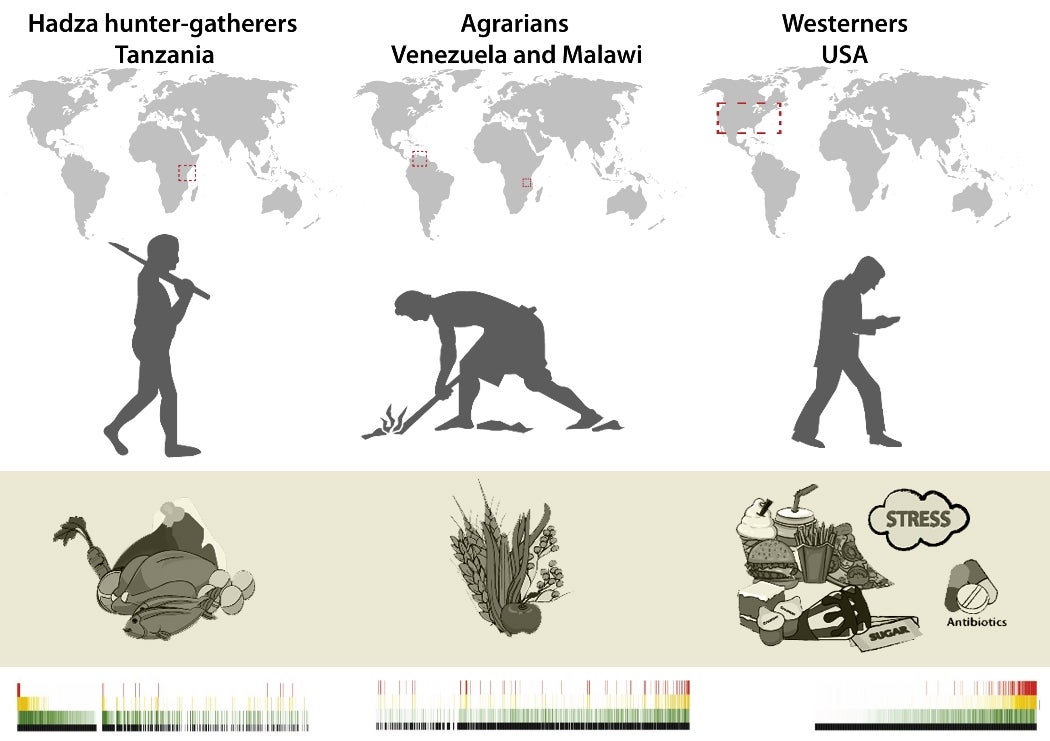
Grafik: Mod. nach "Schnorr et al. 2014 Nat Comm"
Aber auch zwischen Mitteleuropäern lassen sich Unterschiede erkennen. Eine ballaststoffreiche Ernährung kann man beispielsweise von einer Fast-Food-lastigen an bestimmten Bakteriensignaturen differenzieren. Bei der Fast-Food-reichen Ernährung fehlen klassische ballaststoffabbauende Bakterien, und deren Metaboliten sucht man vergeblich. Ein klassisches Beispiel hierfür ist die Buttersäure. Viel Buttersäure im Darm ist protektiv und antiinflammatorisch, wenig Buttersäure deutet auf eine Ernährung hin, die reich an Zucker und arm an Ballaststoffen ist.
Ein weiteres Beispiel ist die Umstellung auf eine vegane Ernährung. Dabei verschwinden die Laktobazillen im Darm, da diese Laktose als Ernährung benötigen. Dies führt jedoch nicht zu einer funktionellen Veränderung, da andere Bakterien die Aufgaben der Laktobazillen übernehmen, und die Funktionalität der Mikrobiota gewährleisten.
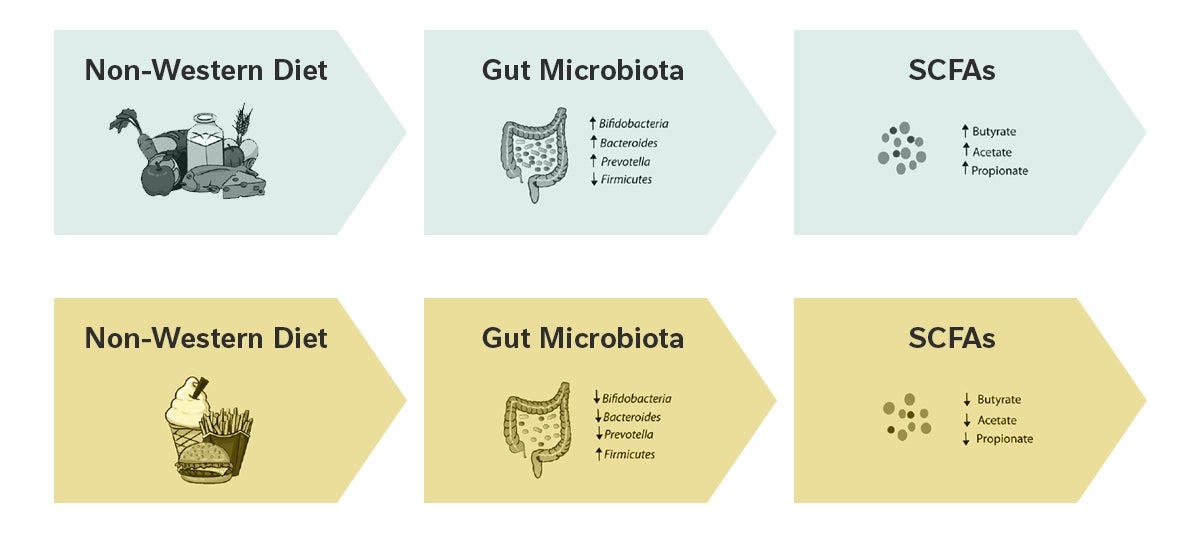
Grafik: Mod. nach "Johnson et al. 2019, Cell Host Microb"
Mittlerweile werden vermehrt Stuhlanalysen für zuhause angeboten, um die Mikrobiota überprüfen zu lassen. Wie stehen Sie dazu?
Grundsätzlich lässt sich sagen, dass Stuhlanalysen für zuhause nur unter ärztlicher Betreuung sinnvoll sind. Ohne eine gründliche Anamnese und Problembeschreibung kann zwar die Bakterienzusammensetzung im Darm aufgezeigt werden, aber keine Rückschlüsse bezüglich der Beschwerden gezogen oder Therapiemaßnahmen vorgeschlagen werden. Einige von diesen Anbietern solcher Tests geben zwar Handlungsempfehlungen, beispielsweise bezüglich der Ernährung, diese sind allerdings in der Regel eher generisch und wenig personalisiert.
Ist es nach einer Antibiotikaeinnahme empfehlenswert, Probiotika einzunehmen, um das gesunde Darmmilieu wiederherzustellen?
Die Probiotika, die auf dem Markt sind, enthalten hauptsächlich Laktobazillen und Bifidobakterien, welche zahlenmäßig im Darm erwachsener Menschen keine entscheidende Rolle spielen. Deren Einnahme führt also kaum zur adäquaten Wiederherstellung des Darmmilieus.
Die Einnahme von Antibiotika führt jedoch dazu, dass Bakterien im Darm absterben. Die bakteriellen Bestandteile gelangen dann an die Darmschleimhaut, woraufhin das Immunsystem reagiert und die Bakterien in Form von Durchfall aus dem Organismus spült. Die Einnahme von Probiotika bereits während der Antibiotikagabe kann helfen, diesen Durchfall zu verhindern, da die Probiotika wie ein Schwamm wirken.
Im Normalfall regelt sich der Wiederaufbau von allein. Eine häufige Antibiotikagabe kann allerdings dazu führen, dass zu viele Bakterien absterben, die dann nur sehr schwer oder gar nicht wiederaufgebaut werden können.
Sehen Sie also einen Zusammenhang zwischen so genannten "Zivilisationskrankheiten" und einer gestörten Mikrobiota?
Es gibt Hinweise darauf, dass die Darmmikrobiota einen Einfluss auf die Entwicklung einer Diabetes-mellitus-Typ-2-Erkrankung hat. Es ist allerdings notwendig, solche Forschungsergebnisse differenziert zu betrachten: Studien deuten zwar auf einen Zusammenhang zwischen einer Antibiotikagabe in jungen Jahren und einer erhöhten Wahrscheinlichkeit für eine spätere Entwicklung einer chronisch entzündlichen Darmerkrankung hin, aber die Entwicklung hängt nicht allein von einer Antibiotikagabe in der Kindheit oder ähnlichen Faktoren ab. Sie ist insbesondere das Ergebnis einer Kombination aus Lebensstil, Ernährung und der damit einhergehenden Darmmikrobiota.
Sie sprachen gerade von einem Zusammenhang von einer gestörten Mikrobiota und Diabetes mellitus Typ 2. Sehen Sie dort das größte Potenzialfeld einer medizinischen Betrachtung des Mikrobioms?
Auf jeden Fall eines der größten. Bei dieser Form des Diabetes sind Ernährung und Lebensstil die größten Stellschrauben. Durch eine mikrobiombewusste Therapie kann in diesem Zusammenhang meines Erachtens viel erreicht werden. Hierzu ist es natürlich zunächst einmal notwendig, sowohl in der Bevölkerung als auch beispielsweise bei behandelnden Ärzten ein Bewusstsein für die Zusammenhänge zu schaffen. Leider ist das Thema Mikrobiom für viele Ärzte noch nicht ausreichend präsent, insbesondere fehlen aktuell noch konkret formulierte Therapieoptionen. Das ist meiner Meinung nach ein wichtiger Ansatzpunkt, damit das Thema Mikrobiom zugänglicher wird und für Ärzte und Patienten an Bedeutung gewinnen kann.

1990 – 1996 Studium der Biologie in Oldenburg, Cork (Irland) und St. Petersburg (Russland), 1997 – 2000 Wissenschaftlicher Mitarbeiter am Deutschen Institut für Ernährungsforschung (DIfE), Potsdam-Rehbrücke, 2000 Promotion zum Dr. rer. nat., 2001 – 2002 Wissenschaftlicher Mitarbeiter am DIfE, seit 2003 Leiter der Abteilung Forschung und Entwicklung am MVZ Institut für Mikroökologie Herborn, 2012 Habilitation und venia legendi für das Fach Gastrointestinale Mikrobiologie an der Justus-Liebig-Universität, Gießen.
Zahlreiche Veröffentlichungen und Buchbeiträge in nationalen und internationalen Fachzeitschriften. 2002 Marie Curie Forschungs- und Reisestipendium der EU. Von 2008 bis 2013 Mitglied in der Kommission für Biologische Gefahren am Bundesinstitut für Risikobewertung (Berlin, Deutschland). Seit 2014 Mitglied des wissenschaftlichen Beirats der Hochschule Furtwangen und der Old Herborn University, Herborn.




